กรดและเบสเป็นแนวคิดพื้นฐานสองประการในเคมีที่มีการประยุกต์ใช้ในวงกว้างในวิทยาศาสตร์ อุตสาหกรรม และชีวิตประจำวัน การทำความเข้าใจว่ากรดและเบสคืออะไร
ปฏิกิริยาของกรดและเบสมีปฏิสัมพันธ์กันอย่างไร และความสำคัญของกรดและเบสในกระบวนการต่างๆ จะช่วยให้เข้าใจโลกของเคมีได้อย่างลึกซึ้งยิ่งขึ้น
บทความที่ครอบคลุมนี้ เราจะอธิบายรายละเอียดคำจำกัดความ คุณสมบัติ และตัวอย่างของกรดและเบส รวมถึงความสำคัญของกรดและเบสทั้งในบริบททางทฤษฎีและทางปฏิบัติ
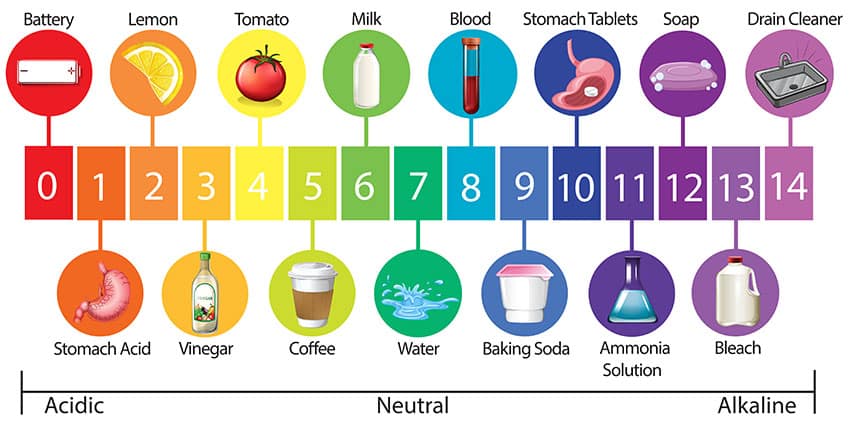
กรดคืออะไร?
กรด (Acid) คือสารที่สามารถบริจาคโปรตอน (ไฮโดรเจนไอออน H+) ให้กับสารอื่น กรดมีลักษณะเฉพาะคือสามารถเพิ่มความเข้มข้นของไฮโดรเจนไอออนในสารละลาย ซึ่งส่งผลให้ค่า pH ต่ำลง ความเข้มข้นของกรดขึ้นอยู่กับความสามารถในการแยกตัวและบริจาคไอออน (H+) ในสารละลาย

คุณสมบัติทั่วไปของกรด:
- รสเปรี้ยว: กรดหลายชนิดมีรสเปรี้ยว ตัวอย่างเช่น กรดซิตริกทำให้เลมอนและผลไม้รสเปรี้ยวอื่นๆ มีรสเปรี้ยว
- การกัดกร่อน: กรดที่มีฤทธิ์กัดกร่อนสูง เช่น กรดไฮโดรคลอริก (HCl) อาจกัดกร่อนได้รุนแรงและสามารถทำลายโลหะและเนื้อเยื่ออินทรีย์ได้
- การทำปฏิกิริยากับโลหะ: กรดทำปฏิกิริยากับโลหะเพื่อผลิตก๊าซไฮโดรเจนและเกลือ ตัวอย่างเช่นเมื่อกรดไฮโดรคลอริกทำปฏิกิริยากับสังกะสี จะผลิตสังกะสีคลอไรด์และก๊าซไฮโดรเจน
- ค่า pH น้อยกว่า 7: กรดมีค่า pH ต่ำกว่า 7 โดยกรดที่มีฤทธิ์กัดกร่อนสูงจะมีค่า pH ต่ำกว่า

ตัวอย่างของกรด:
- กรดไฮโดรคลอริก (HCl): พบในกรดในกระเพาะอาหาร ช่วยในการย่อยอาหาร
- กรดซัลฟิวริก(H2SO4): ใช้ในแบตเตอรี่รถยนต์และกระบวนการทางอุตสาหกรรม
- กรดอะซิติก (CH3COOH): ส่วนประกอบหลักของน้ำส้มสายชู
- กรดซิตริก (C6H8O7): พบในผลไม้รสเปรี้ยวและใช้เป็นสารกันบูดในอาหารและเครื่องดื่ม
ด่าง (เบส) คืออะไร?
ด่าง (Alkaline) คือสารที่สามารถรับโปรตอน (รับไฮโดรเจนไอออน H+) หรือบริจาคอิเล็กตรอนวาเลนซ์คู่หนึ่งเพื่อสร้างพันธะ เบสมีลักษณะเฉพาะคือความสามารถในการเพิ่มความเข้มข้นของไอออนไฮดรอกไซด์ (OH⁻) ในสารละลาย
ซึ่งส่งผลให้ค่า pH สูงขึ้น ความแรงของด่างขึ้นอยู่กับความสามารถในการแตกตัวและปลดปล่อยไอออนไฮดรอกไซด์ในสารละลาย
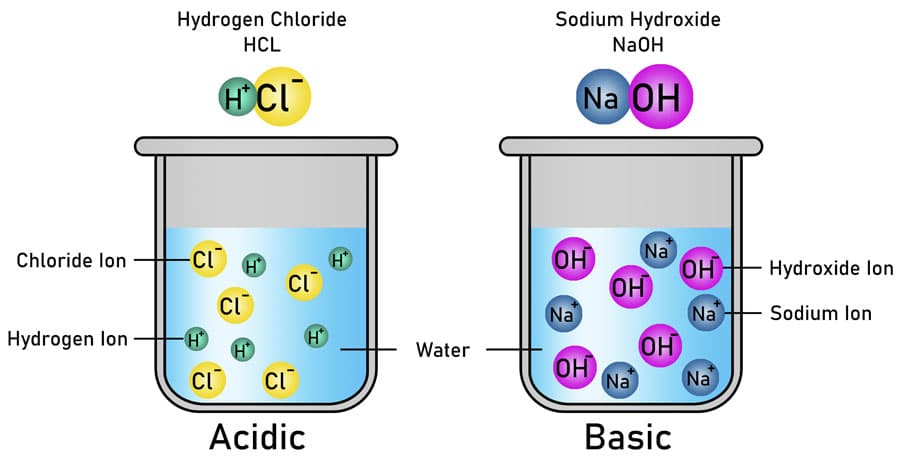
คุณสมบัติทั่วไปของด่าง:
- รสขม: เบสมักจะมีรสขม แต่ไม่แนะนำให้ชิมเนื่องจากอาจเป็นพิษได้
- สัมผัสลื่น: เบสมักจะรู้สึกลื่นเมื่อสัมผัสเนื่องจากทำปฏิกิริยากับน้ำมันบนผิวหนังเพื่อสร้างสารคล้ายสบู่
- ความสามารถในการทำให้กรดเป็นกลาง: เบสทำปฏิกิริยากับกรดเพื่อผลิตน้ำและเกลือ ซึ่งเป็นกระบวนการที่เรียกว่าการทำให้เป็นกลาง
- ค่า pH มากกว่า 7: เบสมีค่า pH สูงกว่า 7 โดยเบสที่เข้มข้นกว่าจะมีค่า pH ที่สูงกว่า

ตัวอย่างของเบส:
- โซเดียมไฮดรอกไซด์ (NaOH): เรียกกันทั่วไปว่าโซดาไฟ ใช้ในการทำสบู่และน้ำยาล้างท่อ
- แอมโมเนีย (NH3): ใช้ในน้ำยาทำความสะอาดในครัวเรือนและปุ๋ย
- แคลเซียมไฮดรอกไซด์ (Ca(OH)2): รู้จักกันในชื่อปูนขาว ใช้ในการก่อสร้างและบำบัดดินที่เป็นกรด
- แมกนีเซียมไฮดรอกไซด์ (Mg(OH)2): ส่วนผสมในยาลดกรดและยาระบาย
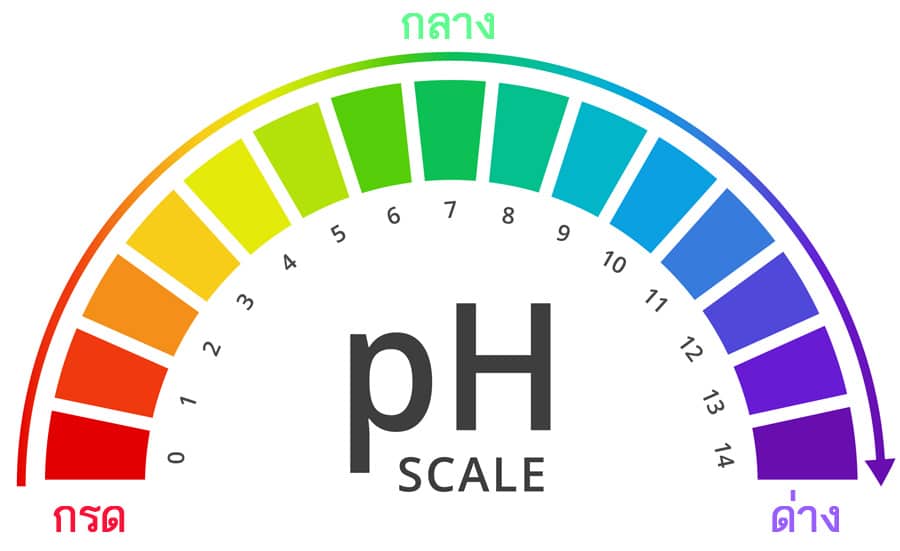
pH: การวัดความเป็นกรดและด่าง
มาตราส่วน pH ใช้ในการวัดความเป็นกรดหรือด่างของสารละลาย โดยมีช่วงตั้งแต่ 0 ถึง 14:
- pH 7: เป็นกลาง (น้ำบริสุทธิ์)
- pH < 7: เป็นกรด โดยตัวเลขที่ต่ำกว่าแสดงถึงความเป็นกรดที่เข้มข้นกว่า
- pH > 7: เบส (ด่าง) โดยตัวเลขที่สูงขึ้นแสดงถึงความเป็นด่างที่เข้มข้นกว่า
มาตราส่วน pH เป็นลอการิทึม ซึ่งหมายความว่าการเปลี่ยนแปลงแต่ละหน่วยแสดงถึงการเปลี่ยนแปลงสิบเท่าในความเข้มข้นของไอออน (H+) ตัวอย่างเช่น สารละลายที่มีค่า pH 3 จะมีความเป็นกรดมากกว่าสารละลายที่มีค่า pH 4 ถึง 10 เท่า
ทำความเข้าใจเพิ่มเติมค่า pH คืออะไร คำอธิบายง่ายๆ ทำความเข้าใจพื้นฐานกรดและด่าง
วิธีการวัดค่ากรด-ด่างได้อย่างไร
มีหลายวิธีในการวัดค่า pH ขึ้นอยู่กับความแม่นยำที่ต้องการ:
1. แถบวัดค่า pH (Test strips): แถบวัดค่า pH เป็นกระดาษที่ชุบด้วยสีย้อมที่ไวต่อค่า pH เมื่อจุ่มลงในสารละลาย แถบจะเปลี่ยนสีตามค่า pH ของสารละลาย แถบวัดค่า pH เป็นวิธีที่รวดเร็วและง่ายดายในการประมาณค่า pH แม้ว่าจะไม่แม่นยำเท่ากับวิธีอื่นๆ ก็ตาม

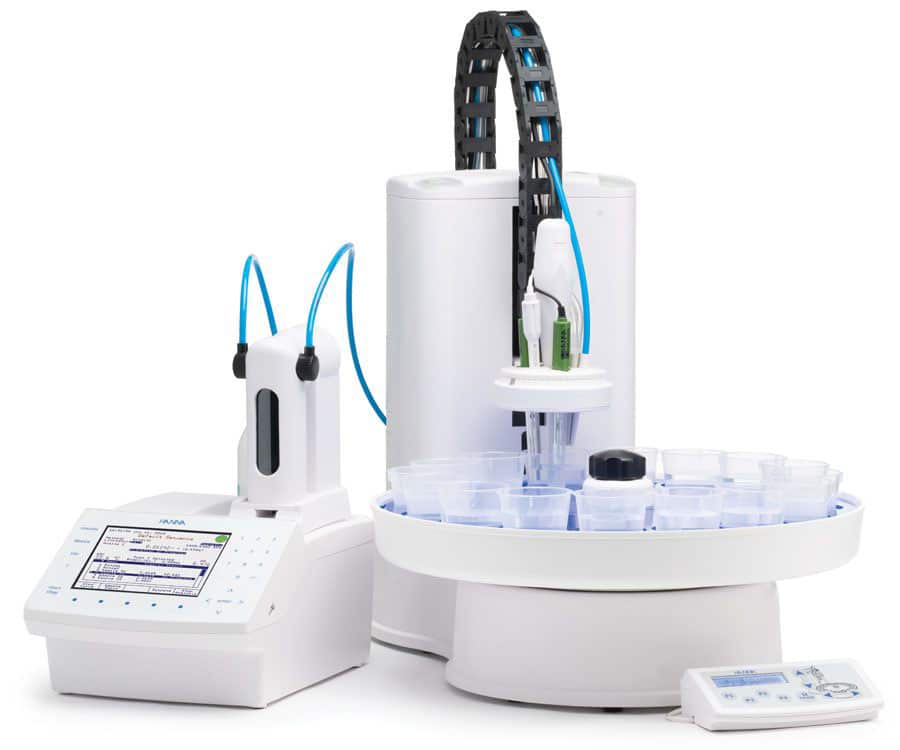
2. pH Meter: เครื่องวัดค่า pH เป็นอุปกรณ์อิเล็กทรอนิกส์ที่วัดความเข้มข้นของไอออนไฮโดรเจนในสารละลาย ประกอบด้วยหัววัด (อิเล็กโทรดแก้ว) ที่ไวต่อไอออนไฮโดรเจน และเครื่องวัดดิจิทัลที่แสดงค่า pH
เครื่องวัดค่า pH ให้ค่าการอ่านที่แม่นยำสูงและมักใช้ในห้องปฏิบัติการ โรงงานอุตสาหกรรม และการทดสอบคุณภาพน้ำ

3. การไทเทรต: ในห้องปฏิบัติการ สามารถวัดค่า pH ได้โดยการไทเทรต โดยเติมสารละลายที่มีความเข้มข้นที่ทราบลงในสารละลายที่มีค่า pH ที่ไม่ทราบค่า จนกระทั่งเกิดปฏิกิริยาที่บ่งชี้ระดับ pH ที่เฉพาะเจาะจง วิธีนี้มีความแม่นยำและมักใช้ในการวิเคราะห์ทางเคมี
ความสำคัญของกรดและเบสในชีวิตประจำวัน
กรดและเบสเป็นส่วนสำคัญในชีวิตประจำวันและในอุตสาหกรรมต่างๆ
- ระบบชีวภาพ: ร่างกายมนุษย์ต้องอาศัยสมดุลกรด-เบสเพื่อให้ทำงานได้อย่างถูกต้อง ตัวอย่างเช่น เลือดมีค่า pH ประมาณ 7.4 การเบี่ยงเบนจากค่า pH นี้อาจนำไปสู่ปัญหาสุขภาพที่ร้ายแรง
- การเกษตร: ค่า pH ของดินมีความสำคัญต่อการเจริญเติบโตของพืช พืชผลส่วนใหญ่มักต้องการค่า pH ที่เป็นกรดเล็กน้อยถึงเป็นกลาง ดินที่มีค่า pH เป็นกรดหรือด่างมากเกินไปอาจทำให้ขาดสารอาหาร
- อาหารและเครื่องดื่ม: กรด เช่น กรดซิตริกและกรดอะซิติก ใช้ในการถนอมอาหารและเพิ่มรสชาติ ส่วนเบส เช่น โซเดียมไบคาร์บอเนตใช้ในการอบ
- ผลิตภัณฑ์ทำความสะอาด: ผลิตภัณฑ์ทำความสะอาดในครัวเรือนหลายชนิดเป็นเบส เนื่องจากเบสสามารถสลายไขมันและสิ่งสกปรกได้อย่างมีประสิทธิภาพ
- การใช้งานในอุตสาหกรรม: กรดและเบสใช้ในกระบวนการอุตสาหกรรมต่างๆ มากมาย รวมถึงการผลิต ยา และการผลิตสารเคมี

สรุป
กรดและเบสเป็นองค์ประกอบพื้นฐานของเคมี ซึ่งมีความหมายกว้างไกลในทางวิทยาศาสตร์ อุตสาหกรรม และชีวิตประจำวัน เมื่อเราเข้าใจแล้วว่ากรดและเบสคืออะไร
คุณสมบัติของกรดและเบส และปฏิกิริยาระหว่างกรดและเบสจะช่วยให้เราเข้าใจกระบวนการทางเคมีที่เกิดขึ้นรอบตัวเราได้ดีขึ้น ไม่ว่าจะอยู่ในห้องทดลอง ในธรรมชาติ หรือในร่างกายของเราเอง กรดและเบสมีบทบาทสำคัญในการรักษาสมดุลและอำนวยความสะดวกในการเกิดปฏิกิริยาเคมี
บทความที่เกี่ยวข้อง
- ออกซิเดชัน (Oxidation) คืออะไร? ทำความเข้าใจพื้นฐาน
- ค่า TDS มาตรฐานในน้ำคืออะไร? สำหรับคุณภาพน้ำที่ควรรู้
- คลอรีนมีประโยชน์อย่างไร? คู่มือฉบับสมบูรณ์
- ทำความเข้าใจความกระด้างของน้ำคืออะไร: คู่มือฉบับสมบูรณ์

